-
La Direttiva 2017/745 (ex 93/42/CEE), definisce le condizioni per l'immissione in commercio dei Dispositivi Medici con la finalità di garantire la sicurezza e la protezione della salute dei pazienti, degli utilizzatori e di eventuali terzi durante l’uso di tali prodotti.
- i dispositivi medicali (in genere) - Direttiva 93/42/CE (MDD)
- i dispositivi diagnostici in vitro - Direttiva 98/79/CE (IVD)
- i dispositivi medici impiantabili attivi - Direttiva 90/385/CE
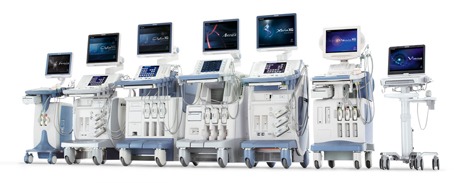
I Dispositivi Medici sono una categoria di prodotti (strumenti, apparecchi, impianti, sostanze, software o altro) destinati ad essere impiegati nell’uomo o sull’uomo a scopo di diagnosi, prevenzione, controllo o terapia, attenuazione o compensazione di ferite o handicap, ma anche di studio, sostituzione o modifica dell’anatomia o di un processo fisiologico, o di controllo del concepimento.
Per essere venduti all'interno dell'Unione Europea, i prodotti devono essere conformi alle direttive di prodotto pertinenti ed essere marcati CE. I requisiti per i dispositivi medici sono più restrittivi rispetto alla maggior parte delle altre categorie, ed in molti casi il produttore si deve obbligatoriamente rivolgere ad un Organismo Notificato per apporre il marchio CE sul proprio dispositivo.
Un prodotto può essere considerato Dispositivo Medico se svolge la propria azione principale attraverso mezzi che non siano farmacologici, immunologici o metabolici, ma la cui funzione possa essere, eventualmente, coadiuvata da tali mezzi (azione ancillare). La destinazione d'uso del prodotto deve essere comunque sempre connotabile come una finalità medica.
La Direttiva 2017/745 (ex 93/42/CEE) raggruppa i Dispositivi Medici in funzione della loro complessità e del potenziale rischio per il paziente, in quattro classi: I, IIa, IIb, III (Annex IX della Direttiva MDD), che si differenziano in base alla destinazione d’uso del dispositivo ed al suo rischio.
Direttive Comunitarie Dispositivi Medicali 2017/745:
La classificazione dipende dalla destinazione d’uso indicata dal fabbricante; tuttavia i dispositivi medici di cui ci occupiamo sono quelli della Classe I.
Classe I: dispositivi a basso rischio. Possono essere prodotti per l'aiuto esterno del paziente, come stampelle o sedie a rotelle ma anche prodotti come stetoscopi. I dispositivi che ricadono in questa classe non richiedono l'intervento di un Organismo Notificato (a parte i dispositivi sterili e/o con funzione di misura) e devono essere registrati presso le autorità locali di competenza.